Варикоцеле – симптомы и лечение
Что такое варикоцеле? Причины возникновения, диагностику и методы лечения разберем в статье доктора Рыжкова Алексея Игоревича, андролога со стажем в 14 лет.


Определение болезни. Причины заболевания
Варикоцеле представляет собой варикозное расширение вен в мошонке, по которым кровь должна оттекать от яичка. В 96% случаев этот процесс наблюдается в левой половине мошонки, значительно реже — с обеих сторон, и очень редко — в правой половине. [1] Изменения вен яичка аналогичны происходящим при варикозном расширении вен на ногах — вены увеличиваются в диаметре, приобретают характерную извитость.
Варикоцеле — весьма распространённое состояние, наблюдается у 11,7% взрослых мужчин. [2] Предпосылки для развития варикоцеле закладываются с рождения, но появляется оно в подростковом возрасте, именно в этот период яички увеличиваются в размере и начинают активно функционировать.
Причина варикоцеле заключается во врождённых особенностях строения сосудистой системы организма, приводящих к высокому давлению в венозных сосудах, собирающих кровь от яичка. Именно поэтому варикоцеле чаще возникает слева, так как вена левого яичка впадает в левую почечную вену под прямым углом, способствуя созданию неблагоприятных условий для оттока венозной крови от яичка. Вена правого яичка впадает под острым углом в нижнюю полую вену, что значительно реже нарушает ток венозной крови.
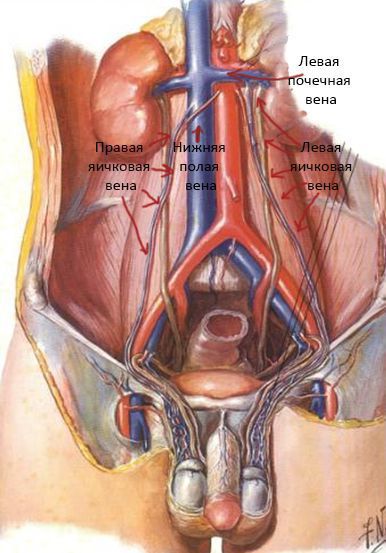
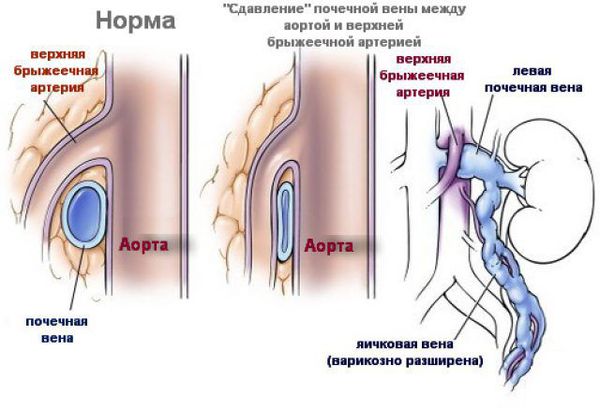
Чаще всего (76% случаев) повышается давление в левой почечной вене, так как она сдавливается между аортой и артерией, отходящей от аорты к кишечнику. Данное состояние называется аорто-мезентериальный пинцет. Эта аномалия часто наблюдается у высоких и худых мужчин, что объясняет более частое наличие у них варикоцеле. [3]
Значительно реже (в 17% случаев) варикоцеле возникает, когда повышается давление в левой общей подвздошной вене вследствие её сдавления между правой общей подвздошной артерией и позвоночником. Данное состояние называется синдром Мейя-Тернера.
Ещё одна причина возникновения варикоцеле — врождённая слабость сосудистой стенки, даже когда отсутствует высокое давление в крупных венозных сосудах, происходит прогрессирующее нарушение венозного оттока от яичка. Тогда варикоцеле часто сочетается с другими заболеваниями вен: варикозная болезнь ног, геморрой.
Изредка варикоцеле бывает вторичным, т.е. возникает не в пубертатном, а в более зрелом возрасте (чаще после 40 лет). В этом случае нужно исключать опухолевые заболевания почки, которые могут сопровождаться формированием опухолевого тромба, нарушающего отток венозной крови в почечной или нижней полой вене и за счёт этого приводящие к формированию варикоцеле. В 9% случаев наблюдается сочетание двух этих механизмов формирования варикоцеле.
Определенную роль в возникновении данных сосудистых аномалий играет наследственность. Варикоцеле у отца повышает вероятность наличия этого заболевания у сына в 4-8 раз. [4]
Симптомы варикоцеле
Как правило, варикоцеле протекает бессимптомно и выявляется случайно при обследовании у уролога.
Болевые ощущения в мошонке наблюдаются у 2-11% мужчин с варикоцеле. [5]
Боль при варикоцеле может иметь различную интенсивность: от лёгкого дискомфорта до сильной боли. Характерно, что боль возникает или усиливается на фоне физической нагрузки, особенно продолжительной. Это связано с дополнительным обратным сбросом венозной крови в вены мошонки при повышении давления в брюшной полости. Как правило, боль снижается и проходит, если пациент принимает горизонтальное положение.
При варикоцеле размеры мошонки могут увеличиваться, заболевание может приводить к деформации ее контура, что может стать существенным косметическим дефектом для молодых мужчин.
Патогенез варикоцеле
Увеличение сопротивления венозному оттоку приводит к тому, что яичковые вены расширяются, разрушается клапанный аппарат и происходит обратный ток венозной крови по ним. В этой ситуации сосудистая система яичка и семенного канатика переполняется венозной кровью, приводя к снижению артериального притока к яичку и нарушению его кровоснабжения. При значительном нарушении кровотока яичко уменьшается в размерах (гипотрофия), менее значимые изменения нарушают его функцию: первоначально это нарушение продукции сперматозоидов, а в последующем снижается выработка половых гормонов.
Важным моментом является то, что на фоне скопления в мошонке тёплой венозной крови происходит повышение её температуры. Общеизвестно, что яички у мужчин неслучайно вынесены наружу, это необходимо для адекватного протекания сперматогенеза. Мошонка в данном случае выполняет функцию термостата, приближая и отдаляя яички от тела, она поддерживает их температуру на оптимальном уровне 34-35℃. Многочисленными исследованиями с использованием теплометрии было доказано, что температура мошонки на фоне варикоцеле поднимается до 36-37℃, что негативно сказывается на сперматогенезе.
Многие пациенты задаются вопросом, почему при варикоцеле, выявленном с одной стороны (преимущественно слева), страдают оба яичка. Это объясняется тем, что из-за варикоцеле происходит повышение температуры всей мошонки, при этом нарушается сперматогенез в соседнем яичке.
Еще один механизм негативного влияния варикоцеле на яички связан со сбросом в яичко большого количества гормонов надпочечников, концентрация которых в почечной вене велика за счёт впадения в нее надпочечниковых вен. Гормоны надпочечников обладают негативным влиянием на сперматогенез, а их высокая концентрация в венах яичка при варикоцеле была доказана в ряде исследований.
Классификация и стадии развития варикоцеле
Сегодня используется классификация Всемирной Организации Здравоохранения, предложенная в 1997 г. и включающая 4 степени:
- III степень – расширенные венозные сплетения выпячиваются сквозь кожу мошонки и легко прощупываются;
- II степень – расширенные вены в мошонке не видны, но легко прощупываются;
- I степень – расширенные вены не видны и не прощупываются, за исключением их расширения при ман`вре Вальсальвы (проба с натуживанием, приводящая к повышению давления внутри брюшной полости и сбросу венозной крови в мошонку);
- Субклиническая степень – нет признаков варикоцеле при осмотре, но оно выявляется при ультразвуковом исследовании в допплеровском режиме.
Кроме этого, варикоцеле подразделяют на три гемодинамических типа, согласно рассмотренным ранее причинам:
- Реносперматический тип – отмечается обратный ток венозной крови из почечной вены в вены яичка;
- Илеосперматический тип – имеется обратный ток венозной крови из подвздошных сосудов в вены яичка;
- Смешанный тип (комбинация реносперматического и илеосперматического типа варикоцеле).
Осложнения варикоцеле
Возможные осложнения варикоцеле включают в себя:
- мужское бесплодие;
- гипотрофию яичка;
- мужской гипогонадизм.
Под бесплодием понимают отсутствие беременности на протяжении более 1 года у пары, регулярно живущей половой жизнью без использования средств контрацепции. Бесплодие — самое частое патологическое состояние, наблюдаемое у мужчин с варикоцеле, а в структуре причин мужского бесплодия варикоцеле находится на первом месте.
Наибольшую информацию о степени влияния варикоцеле на способность к зачатию даёт исследование спермы (спермограмма). Изменения спермограммы при варикоцеле варьируют в широких пределах: от полного отсутствия сперматозоидов (азооспермия), наблюдаемого в редких случаях, до умеренных нарушений подвижности сперматозоидов (астенозооспермии). Кроме этого, варикоцеле может быть причиной положительного MAR-теста (тест на иммунное бесплодие). Многочисленные исследования продемонстрировали, что излечение варикоцеле приводит к значительному увеличению шансов на зачатие, что подтверждает роль варикоцеле в возникновении бесплодия.
О гипотрофии яичка говорят в тех случаях, когда яичко уменьшено в объёме более чем на 10% по сравнению с противоположным. Данные о частоте этого состояния у мужчин с варикоцеле варьируют в широких пределах от 10 до 77%. [6] [7] Причиной гипотрофии является нарушение кровоснабжения яичка на фоне варикоцеле. В большинстве, хотя и не во всех случаях, излечение варикоцеле приводит к восстановлению нормального объёма яичка.
Мужской гипогонадизм представляет собой снижение уровня мужских половых гормонов, в первую очередь тестостерона, до уровня ниже нормальных значений. Симптомы данного состояния весьма разнообразны. Это и сексуальные расстройства в виде нарушений эрекции, утраты сексуального желания, и психоэмоциональные изменения в виде снижения работоспособности, концентрации, а также уменьшение количества мышечной массы, увеличение количества жировой ткани и др.
В норме у мужчин тестостерон начинает снижаться примерно с 30 лет по 1-2% в год. При наличии варикоцеле, как было показано в ряде исследований, этот процесс может протекать значительно быстрее, и, в целом, мужчины с варикоцеле имеют более низкий уровень тестостерона по отношению к здоровым мужчинам. Причина этого состояния, с большой вероятностью, также связана с нарушением кровоснабжения в яичке в результате варикоцеле, что приводит к снижению активности ферментов, участвующих в синтезе тестостерона, и закономерно снижает его концентрацию. Излечение варикоцеле позволяет надеяться на повышение концентрации тестостерона в крови.
Диагностика варикоцеле
Постановка диагноза варикоцеле производится на основании осмотра пациента, но диагноз должен обязательно подтверждаться ультразвуковым исследованием с допплерографией сосудов мошонки.
Ультразвуковое исследование позволяет определить наличие варикозных вен лозовидного сплетения мошонки и оценить их диаметр. Расширение вен лозовидного сплетения на ширину 2,5 мм или более позволяет поставить пациенту диагноз варикоцеле. Кроме этого, при УЗИ обязательно оценивают состояние яичка и его размеры, чтобы установить возможность гипотрофии.
Ультразвуковое исследование нужно дополнять допплерографией. Этот режим позволяет оценить направление тока крови по венам. В норме кровь по венам должна оттекать от яичка, если же имеет место обратный ток крови к яичку в покое или во время пробы Вальсальвы, можно констатировать наличие у пациента варикоцеле.
Лечение варикоцеле
Лечение варикоцеле только оперативное, никакие другие методы лечения, включая коррекцию образа жизни и приём лекарственных препаратов, не являются эффективными.
Хирургическое лечение варикоцеле показано при наличии:
- боли в мошонке;
- гипотрофии яичка;
- мужском бесплодии.
За всю историю лечения варикоцеле было предложено более 300 различных оперативных пособий.
Сегодня используются четыре вида операций:
- операция Иваниссевича;
- лапароскопическая венэктомия;
- рентгенэндоваскулярная окклюзия яичковой вены.
- микрохирургическая субингвинальная варикоцелэктомия
Все представленные методы лечения направлены на блокирование обратного тока венозной крови за счёт максимально эффективного пересечения яичковых вен на разных уровнях.
Операция Иваниссевича — наиболее простой и наименее эффективный способ лечения варикоцеле. Выполняется разрез в подвздошной области слева, в забрюшинном пространстве находится яичковая вена, представленная одним или двумя-тремя стволами, перевязывается и пересекается. Преимущества операции — в простоте исполнения; недостатки — высокая травматичность, плохой косметический результат (разрез 5-7 см) и очень большая частота осложнений, например, рецидив варикоцеле (повторное возникновение варикоцеле) — 29% и гидроцеле (водянка, скопление большого количества жидкости между оболочками мошонки, увеличивающее её объём и требующее оперативного лечения) — 5-10%. [8]
Лапароскопическая венэктомия отличается от операции Иваниссевича тем, что для доступа к яичковой вене используется эндоскопическая техника. На передней поверхности живота делаются небольшие разрезы (3 по 1,5 см), через которые в брюшную полость вводится камера и эндоскопические инструменты, с помощью которых находится, выделяется, клипируется и пересекается яичковая вена. К преимуществам данной методики следует отнести лучший по отношению к операции Иваниссевича косметический эффект. К недостаткам — достаточно высокий риск развития рецидива (7%) и гидроцеле (5,8%), а также возможность развития тяжёлых осложнений, связанных с проникновением в брюшную полость (травма кишечника, крупных сосудов и нервов, лёгочная эмболия, перитонит, послеоперационная боль в правом плече (из-за диафрагмального растяжения во время пневмоперитонеума). [8]
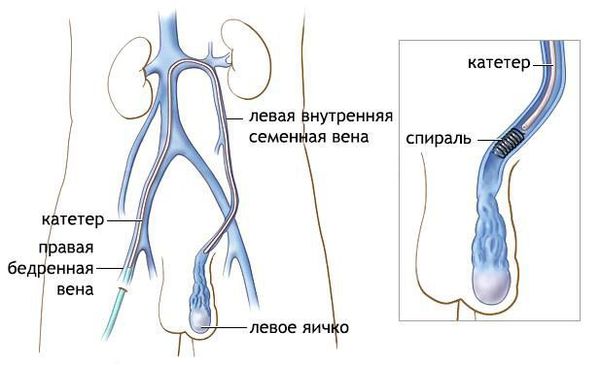
Эндоваскулярная эмболизация яичковой вены — операция, выполняемая не урологами, а сосудистыми хирургами. Под местной анестезией выполняется небольшой разрез на бедре, осуществляется доступ в венозную систему. После чего в вену вводится катетер и проводится сначала в почечную, а затем в яичковую вену. На всём протяжении яичковой вены расставляются препятствия току крову в виде спиралей. Преимущества данной методики заключаются в малой травматичности, выполнении процедуры под местной анестезией и отсутствии риска такого осложнения, как гидроцеле. Дело в том, что причиной гидроцеле является случайная перевязка лимфатических сосудов, по которым движется межтканевая жидкость. Данная операция выполняется из просвета вены, что исключает повреждение лимфатических сосудов и, соответственно, развитие гидроцеле. К недостаткам следует отнести лучевую нагрузку (операция выполняется под рентгенологическим контролем), большую частоту неудачных интервенций — 9-27%, т.е. ситуаций, когда хирургу в силу анатомических особенностей не удаеёся дойти до яичковой вены, высокую частоту рецидивов — 10% и других осложнений — 11% (гематомы, перфорации, кровотечения). Сегодня эта методика не используется как метод первичного лечения варикоцеле, она может применяться при рецидиве, когда другие операции не принесли результата.
Микрохирургическая субингвинальная варикоцелэктомия (операция Мармара) — «золотой стандарт» хирургического лечения варикоцеле. При данной методике разрез 2-2,5 см делается на уровне чуть выше основания полового члена. Осуществляется доступ к семенному канатику, который выделяется из окружающих тканей и выводится в рану. Далее под оптическим увеличением вскрывается семенной канатник и разделяются его сосуды, при этом вены перевязываются, а артерия и лимфатические сосуды должны быть сохранены.
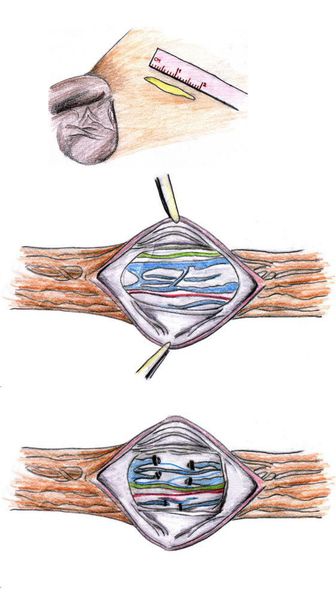
К преимуществам методики относится малая травматичность, хороший косметический результат, низкая вероятность рецидива — 1% и гидроцеле — 0,4%. К недостаткам — сложность выполнения, требующая длительного обучения, и зависимость результата от опыта хирурга (требуется выполнять не менее 100 таких операций в год для обеспечения оптимального результата), а также нарушение артериального кровоснабжения яичка в случае повреждения яичковой артерии, что наблюдается крайне редко (менее 0,01% случаев). [8]
Прогноз. Профилактика
Большинство врачей придерживаются мнения, согласно которому варикоцеле является прогрессирующим заболеванием, постепенно всё более значимо нарушающим функционирование яичек. Этим, в частности, можно объяснить высокую частоту вторичного бесплодия у мужчин с варикцоцеле. В таком случае мужчина с варикоцеле добивается беременности у партнерши в молодом возрасте (до 25 лет), а в последующем, когда пара планирует второго ребенка, возникают трудности, что, вероятно, связано с прогрессирующим нарушением сперматогенеза на фоне варикоцеле. В более позднем возрасте, после 40 лет, варикоцеле распространяет свое влияние на продукцию яичком мужских половых гормонов — функцию гораздо менее чувствительную к негативным факторам, чем сперматогенез. Это может приводить к снижению уровня тестостерона в крови.
Варикоцеле, в подавляющем большинстве случаев, — состояние, предопределённое с рождения, поэтому у нас нет эффективных методов его профилактики. А единственный метод предотвращения прогрессирования заболевания — это его хирургическое устранение.
Варикоцеле
Варикоцеле, впервые описанное Celsius еще в 1-м веке нашей эры, остается до настоящего времени одним из интереснейших и неоднозначно трактуемых урологических заболеваний. Несмотря на то, что Celsius описал его в виде «раздутых и извитых вен над яичком, которое становится меньше противоположного», лишь Bennet W.H. в 1889 установил взаимосвязь между изменениями в мошонке и функциональной недостаточностью яичка.
Согласно Bennet, варикоцеле – это «патологическое состояние вены семенного канатика, возникающее в большинстве случаев в следствие или в сочетании с функциональной недостаточностью яичка». Именно критерий функциональной состоятельности яичек и определяет повышенный интерес клиницистов к данной проблеме, а так же чрезвычайную ее социальную значимость, в особенности для России. Это связано с демографической ситуацией, наблюдаемой в настоящее время в большинстве развитых стран. Не менее 40 % бесплодных браков обусловлено мужским бесплодием. В этой связи проблема распростронения заболевания, которым страдает до 30% мужчин и которое является в 40% -80% случаев причиной снижения фертильности, становится все более актуальной.
Неоднозначность и противоречивость существующих подходов и трактовок отмечается уже на этапе терминологического определения заболевания. В отличие от значительного числа авторов мы придерживаемся мнения, что варикоцеле – это варикозное (гроздьевидное) расширение вен ло-зовидного (plexus pampiniformis) сплетения семенного канатика, сопровож-дающееся интермиттирующим или перманентным венозным рефлюксом (Ковалев В.А., Королева С.В., 2001).
Эпидемиология. Варикоцеле является одним из наиболее распространенных заболеванием среди мужчин , частота встречаемости которого колеблется по данным различных авторов от 2,3% до 30% (Клинические рекомендации, 2007). Имея врожденные предпосылки к развитию, заболеваемость в различных возрастных группах неоднородна. В дошкольном возрасте частота встречаемости не превышает 0,12%. В дальнейшем заболеваемость возрастает по мере роста и взросления. Наиболее часто болезнь встречается в возрасте 15-30 лет, а так же среди спортсменов и работников физического труда. 
Этиология и патогенез. Еще в 1918г. О.Ivanissevitch, определив варикоцеле как «анатомоклинический синдром, анатомически проявляющийся варикозом внутри мошонки, а клиническивенозным рефлюксом, например обусловленным клапанной недостаточностью», связал наличие варикоцеле с недостаточностью клапанов яичковой вены, приводящей к ретроградному кровотоку по ней. В последующем утверждения Иваниссевича нашли подтверждение в связи с широким внедрением в клиническую практику сосудистых исследований, позволяющих визуально оценить состояние внутренней семенной вены на всем ее протяжении. Определяющей на сегодняшний день является концепция, рассматривающая варикоцеле не как самостоятельное заболевание, а как симптом аномалии развития или заболевания нижней полой или почечных вен. (Н.А.Лопаткин 1973). Чрезвычайная вариабельность строения как венозной системы вообще, как левой, так и правой почечной вены является следствием нарушения редукции кардинальных и субкардинальных вен. Ретроградный кровоток наблюдается при врожденном (первичном) отсутствии клапанов в яичковой вене, а так же генетически детерминированной слабости венозной стенки вследствие недоразвития мышечного слоя, дисплазии соединительной ткани, приводящих к первичной клапанной несостоятельности. Вторичная клапанная недостаточность развивается в результате венной гипертензии в системе нижней полой и почечных вен. (Морозов А.В., соавт., 1986). В таких случаях заболевание следует рассматривать в качестве обходного ренокавального анастомоза (через внутреннюю и наружную семенные вены в общую подвздошную), компенсирующего почечную венную гипертензию. Учитывая анатомические особенности, заключающиеся в том, что левая яичковая вена впадает в почечную вену, а правая в большинстве случаев непосредственно в нижнюю полую и лишь в 10 % в правую почечную вену, в структуре заболеваемости преобладает левосто-роннее варикоцеле – 80-86%. Правостороннее варикоцеле встречается в 7-15%, двустороннее в 1-6% случаев.
Вместе с тем, любые патологические состояния на уровне мошонки, пахового канала, брюшной полости (грыжи), почечной и нижней полой вены, приводящие к сдавлению семенных канатиков, повышению внутрибрюшного давления, повышению давления в нижней полой и почечных венах, затрудняющего отток из вен семенного канатика, могут являться причиной рефлюксирующего кровотока и развитию варикоцеле.
В основе перманентного повышения гидродинамического давления в системе почечных вен и перманентного ренотестикулярного рефлюкса ле-жат органические причины – стеноз почечной вены, ретроаортальное расположение левой почечной вены, кольцевидная почечная вена, артериовенозная фистула (Житникова Л.Н. 1978). Варикоцеле в таких случаях определяется как в орто, так и в клиностазе, существует с детства и неуклонно прогрессирует. Особое внимание уделяется интермиттирующему характеру рефлюкса, наиболее часто наблюдаемому при наличии аорто-мезентериального пинцета, являющегося одной из причин наиболее часто встречающегося ортостатического варикоцеле. Заболевание развивается в ряде случаев при опухолях левой почки, опухолях брюшной полости, сдавливающих основные венозные коллекторы, и является в таких случаях симптоматическим с тенденцией к быстрому прогрессированию по мере роста опухоли.
Роль патогенетических факторов, приводящих к нарушениям сперма-тогенеза при варикоцеле, окончательно не установлена. К ним относятся локальная гипертермия, гипоксия, нарушение гематотестикулярного баръера, в том числе с контрлатеральной стороны за счет коллатерального кровотока, приводящее к выработке антиспермальных антител, избыточная продукция кортизола при надпочечниковой венной гипертензии, нарушения рецепторного аппарата и стероидогенеза, нарушения обратной взаимосвязи яички- гипофиз- гипоталамус, местная и общая, относительная и абсолютная андрогенная недостаточность и другие гормональные нарушения в настоящее время продолжает изучаться. В последнее время предметом исследований становиться влияние генетических факторов, приводящих к нарушению сперматогенеза при развитии заболевания (Мазо Е.Б., соавт., 1999). Следует отметить, что прямой коррелятивной связи между степенью выраженности заболевания и степенью нарушения сперматогенеза не существует. Вопрос о влиянии экстрафуникулярного варикоцеле на сперматогенез до настоящего времени изучается. С учетом анатомофизиологических особенностей строения кремастерной вены и поверхностной венозной системы яичка нет единого мнения о патогенетической значимости для гаметогенеза рефлюксирующего типа кровотока, наблюдаемого иногда в норме в данной сосудистой системе.
Профилактика заболевания. Специфической профилактики не существует. Ограничение физических нагрузок не может рассматриваться в качестве рациональной и адекватной меры профилактики.
Классификация.
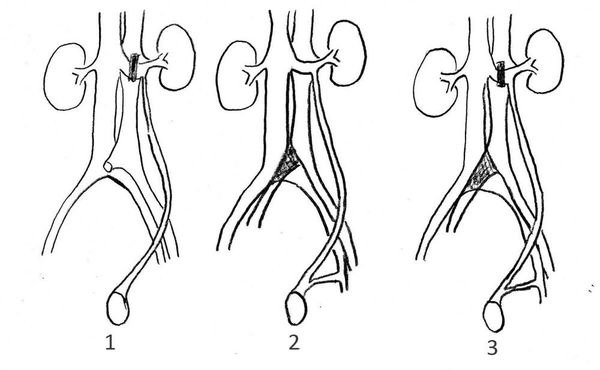
В зависимости от характера флебо-тестикулярных взаимоотношений Coolsaet выделяет три гемодинамических типа рефлюксов (рис 1):
1.Рено-тестикулярный.
2.Илео-тестикулярный.
3.Смешанный.
По степени выраженности существует большое количество классификаций заболевания. Классификация ВОЗ (1997г.)
I степень – расширенные вены выпячивают сквозь кожу мошонки, хо-рошо видны. Яичко уменьшено в размерах, имеет тестоватую консистенцию.
Варикоцеле 2 степени – расширенные вены не видны, но хорошо пальпируются.
Варикоцеле 3 степени – расширенные вены определяются только при пробе Валь-сальвы .
Субклиническое варикоцеле определяется с помощью кашлевого теста или с помощью допплерометрии мошонки с применением пробы Вальсальвы.
В отечественной практике наиболее часто применяется классификация Ю.Ф.Исакова 1977г., основанная на обратной градации проявлений заболе-вания, в отличие от классификации ВОЗ.
I степень- определяется пальпаторно только при пробе Вальсальвы (натуживании) в ортостазе.
II степень- хорошо определяется пальпаторно и визуально. Яичко не изменено.
III степень- выраженная дилятация вен лозовидного сплетения. Яичко уменьшено в размерах, имеет тестоватую консистенцию (Страхов С.Н., 2001).
Диагностика варикоцеле. Субъективно болезнь протекает, как правило, бессимптомно. В некоторых случаях пациенты отмечают тяжесть и болевые ощущения в левой половине мошонки. Следует дифференцировать с воспалительными заболеваниями органов мошонки. Диагноз устанавливается на основе пальпаторного, ультразвукового и допплерографического исследований. Из не инвазивных методов наибольшей чувствительностью обладает ультразвуковое исследование в сочетании с допплерографическим картированием почечных сосудов и яичковой вены. Исследование должно произво-диться в орто- и клиностазе с обязательной оценкой характера изменений (градиента) кровотока (скорость почечного венозного кровотока, скорость и продолжительность тестикулярного рефлюкса) при пробе Вальсальвы и при переводе больного в ортостатическое положение. В норме диаметр яичковой вены на уровне мошонки не превышает 2мм., скорость кровотока не превышает 10 см. в сек., рефлюкс не определяется (Ledda A. Et al. 1996). При субклиническом варикоцеле диаметр яичковой вены увеличивается до 3-4 мм., определяется непродолжительный (до 3 сек.) рефлюкс при пробе Вальсальвы. Дальнейшее увеличение параметров рефлюкса соответствует более выраженным стадиям патологического процесса. Выполнение исследования по описанной методике позволяет в большинстве случаев предположить гемодинамический тип варикоцеле, выявить признаки почечной венной гипертензии и определить субклинические формы заболевания, трудно диагностируемые при пальпации, которая, к тому же является весьма субъективным методом оценки состояния семенного канатика и его элементов. Определенную ценность представляет исследование мочи до и после физической нагрузки. Положительная маршевая проба (появление микрогематурии, протеинурии) свидетельствует о наличии почечной венной гипертензии. Вместе с тем, отрицательная маршевая проба не исключает наличия последней, так как в ряде случаев ренокавальный шунтирующий кровоток через систему яичковых вен бывает достаточным для ее компенсации. В таких случаях маршевая проба может стать положительной после перевязки, клипирования или эмболизации яичковой вены вследствие усугубления почечной венной гипертензии.
Хотя ультразвуковой метод обладает высокой чувствительностью и является на сегодняшний день основным в диагностике заболевания, инвазивные рентгенологические методы отнюдь не утратили своей актуальности и по прежнему обладают наибольшей наглядностью и информативностью. Антеградная флеботестикулография и ретроградная почечная флебография с ретроградной флеботестикулографией и мультипозиционной флеботонометрией должны применяться в неясных случаях и при диагностике рецидивных форм заболевания (рисунки 2,3,4). В ряде случаев обследование должно включать динамическую нефросцинтиграфию с целью определения функционального состояния почек. В зависимости от результатов обследования выбирается вид оперативного вмешательства.
Основными задачами обследования при лечении являются:
1. Определение гемодинамического типа варикоцеле.
2. Оценка степени выраженности почечной венной гипертензии, хара ктера и степени выраженности венозного рефлюкса.
3. Изучение исходного гормонального статуса и сперматогенеза.
Обязательным является семиологическое исследование, МАR-тест, ис-следование гормонального профиля (уровень тестостерона, эстрадиола, про-лактина, ФСГ, ЛГ). У подавляющего большинства пациентов при семиологическом исследовании выявляется патоспермия различной степени выраженности, преимущественно заключающаяся в снижении концентрации активно-подвижных форм сперматозоидов и увеличении количества патологических форм. У 60% больных имеет место олигоспермия.
Пример формулировки диагноза:
1. Ортостатическое левостороннее варикоцеле, II стадия, I гемодинамический тип, олигоастенозооспермия, бесплодный брак.
2. Аортомезентериальный пинцет, интермитирующая почечная венная гипертензия, ортостатическое левостороннее варикоце-ле, III стадия, I гемодинамический тип, астенотератозооспер-мия, бесплодный брак.
Лечение варикоцеле.
Консервативного лечения варикоцеле не существует. Медикаментозная терапия применяется в послеоперационном периоде с целью стимуляции сперматогенеза и включает витамины, биологически активные добавки (селен, цинк) и гормональные препараты (андрогены, хорионический гонадотропин), назначаемые по строгим показаниям курсами под строгим лабораторным контролем.
Известно около 120 видов оперативных вмешательств. Операции, направленные на создание внутреннего суспензория (Франка, Парона), наружного суспензория (Гартмана, Купера) имеют историческое значение. Применяемые в настоящее время пособия подразделяются на две группы
1 группа. Сохраняющие ренокавальный шунт.
К ним относятся шунтирующие операции: проксимальный тестикулоилиакальный и проксимальный тестикуло-сафенный сосудистые анастомозы (рисунок 5). Выполнение двунаправленных анастомозов в настоящее время признано нецелесообразным.
2 группа. Не сохраняющие ренокавальный шунт.
– Супраингвинальные неселективные
Операция A.Palomo (1949) – внутренняя семенная вена перевязывается вместе со всеми сопровождающими сосудистыми структурами.
Операция А.П.Ерохина (1979)– перевязка внутренней семенной вены и артерии с сохранением лимфатических сосудов, для лучшей визуализации которых автор применяет введение раствора индигокармина под белочную оболочку яичка. Бернарди, Кондакова и другие пособия.
– Супраингвинальная селективная
Операция Иваниссевича (1918).
Высокое лигирование яичковой вены.
Операция Speriongano (1999)- перевязка вен у внутреннего кольца пахового канала под контролем интраоперационной цветной допплерсонографии.
– Субингвинальные селективные
Субингвинальное лигирование яичковой вены (микрохирургический метод).
Отдавая предпочтение реконструктивным сосудистым и селективным супра- и субингвинальным вмешательствам, целесообразно использовать оптическое увеличение и прецизионную технику. Выполнение оперативного вмешательства с применением микрохирургической техники позволяет с одной стороны уменьшить количество рецидивов за счет повышения эффективности вмешательства, а с другой стороны уменьшить количество осложнений, связанных с затрудненной дифференцировкой элементов семенного канатика и сосудистых структур, сопровождающих внутреннюю семенную вену.
– Лапароскопическое клипирование яичковой вены
Является эндоскопическим аналогом открытых супраингвинальных вмешательств.
– Эндоваскулярное флебосклерозирование
Выполняется одномоментно с флебографией и флеботонометрией и показано при выявлении 1 гемодинамического типа варикоцеле, отсутствии органического заболевания (стеноз, ретроаортальное расположение почечной вены) и почечной венной гипертензии.
Каждый из перечисленных методов второй группы имеет свои преимущества и недостатки, и их применение при прочих равных условиях в однотипных клинических ситуациях во многом мотивировано индивидуальными предпочтениями хирурга. Принципиальным является выбор между вмешательствами первой и второй группы.
Варикоцеле 1-го гемодинамического типа при наличии органического сужения почечной вены, перманентной или интермиттирующей почечной венной гипертензии с высоким ортостатическим или функциональным (про-ба Вальсальвы) градиентом давления и других параметров ренотестикулярного рефлюкса является показанием к выполнению шунтирующих операций 1 группы.
Прогноз:
Рецидив заболевания отмечается в 2-30 % случаев по данным различных авторов. В среднем рецидивы наступают у 10% оперированных больных и связаны не только с дефектами хирургической техники, но и с ошибочным определением гемодинамического типа варикоцеле. У 90% больных отмечено улучшение показателей сперматогенеза, но лишь у 45% показатели приближались к нормативным. Чем продолжительнее стаж заболевания, чем к более старшей возрастной группе относились оперированные больные, тем этот показатель был ниже и тем более длительным был восстановительный период (до 5-10циклов) у данной категории пациентов.
Заключение:
1.Преобладающим гемодинамическим типом является ренотестикулярный рефлюкс.
2. Оперативное лечение варикоцеле – единственный на сегодняшний день метод лечения этого заболевания.
3.Вид оперативного пособия определяется гемодинамическим типом болезни, наличием почечной венной гипертензии и характером флебо-тестикулярного рефлюкса.
4.Оперативное вмешательство должно предприниматься тогда, когда было выявлено заболевание.
Варикоцеле
РЦРЗ (Республиканский центр развития здравоохранения МЗ РК)
Версия: Клинические протоколы МЗ РК – 2013
Общая информация
Краткое описание
Варикоцеле – варикозное расширение вен гроздьевидного сплетения, развивающееся преимущественно с левой стороны. (Н.А. Лопаткин 1995 г.).
I. ВВОДНАЯ ЧАСТЬ
Название протокола: Варикоцеле
Код протокола:
Код по МКБ-10:
I 86.1 Варикозное расширение вен мошонки. Расширение семенного канатика
Сокращения, используемые в протоколе:
УЗИ- ультразвуковое исследование
Дата разработки протокола: апрель, 2013
Категория пациентов: мужчины от 15 до 40 лет с жалобами на боли и дискомфорт в левой половине мошонки
Пользователи протокола: врачи-урологи, хирурги, андрологи

Автоматизация клиники: быстро и недорого!
– Подключено 300 клиник из 4 стран
– 800 RUB / 4500 KZT / 27 BYN – 1 рабочее место в месяц

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место – 800 RUB / 4500 KZT / 27 BYN в месяц
Мне интересно! Свяжитесь со мной
Классификация
Клиническая классификация: (Лопаткин Н.А. 1998г.):
по стадиям:
– 1 стадия
– 2 стадия
– 3 стадия
по локализации:
– левостороннее
– правостороннее
Диагностика
II. МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
Перечень основных и дополнительных диагностических мероприятий
Основные:
1. Общий анализ крови
2. Общий анализ мочи
3. Коагулограмма крови
4. Определение группы крови и резусфактора
5. Осмотр анестезиолога (детям до 14 лет)
6. ЭКГ
7. УЗИ мочевыделительной системы, яичек и вен гроздьевидного сплетения
Дополнительные:
1. Определение мочевины и остаточного азота
2. Определение глюкозы
3. Определение билирубина
4. Спермограмма ( старше 18 лет) при наличии бесплодия
5. Гормоны(тестостерон, ФСГ,ЛГ,пролактин) при наличии бесплодия
Диагностические критерии: (Лопаткин Н.А.1998 г.)
Жалобы и анамнез:
– на наличие варикозно трасширенных вен семенного канатика
Физикальные данные:
– наличие варикозно трасширенных вен семенного канатика, определяемых при осмотре
Лабораторные исследования:
– наличие изменений спермограммы (астенозооспермия- снижение фертильности)
Инструментальные исследования:
– УЗИ: наличие варикозно расширенных вен семенного канатика больше 2,0-2,5 мм
– почечная венография: позволяет установить механизм возникновения варикоцеле ( извращение кровотока по яичниковой вене под действием гидростатического фактора, либо венной застойной гипертензии.).
Дифференциальный диагноз
| Признаки | Варикоцеле | Орхоэпидидимит |
| Объективные данные | Наличие варикозно расширенных вен семенного канатика. Проба Вальсальвы. | Внезапно возникающие боли в яичке, озноб, повышение температуры тела до 38-39, увеличение яичка. |
| УЗИ | Наличие варикознорасширенных вен гроздьявидного сплетения. | Придаток яичка утолщен, возникает периорхит и реактивная водянка. |
| Дополнительные методы. | Почечная венография- извращение кровотока по яичниковой вене. | Нет. |
| ОАК | В пределах нормы | Лейкоцитоз- наличие признаков воспаления |
Лечение
Цель лечения: Перевязка и пересечение левой яичниковой вены, что прерывает обратный ток крови из почечной вены в гроздьевидное сплетение.
Тактика лечения
Немедикаментозное лечение: режим стационарный, стол №15.
Медикаментозное лечение:
1. Антибиотики цефалоспоринового ряда – цефотоксим (цефазолин) 1,0* 2 р/д
2. Уросептики фторхинолонового ряда: офлоксацин 400 мг 2 р/д
3. Анальгезирующие препараты (кетопрофен 2,0 в/м, анальгин 1,0, дротаверин 2,0 в/м)
4. Улучшающие микроциркуляцию: пентоксифиллин в/в капельно
5. Противогрибковые: итраконазол оральный раствор150 мл-10 мгмл по 100 мг 2 раза в день, флуконазол 150 мг 1 раз
6. Витамины С (аскорбиновая кислота)
Другие виды лечения: нет
Оперативное лечение:
1. Операция:субингвинальное микрохирургическое устранение варикоцеле.
2. Операция: рентгенэндоваскулярное склерозирование (РЭС) левой яичниковой вены при рецидивах варикоцеле.
Профилактические мероприятия:
– избегать переохлаждений;
– при необходимости проведение противовоспалительной терапии, с целью санации хронических очагов инфекции мочевой системы в периоды между этапами оперативного лечения.
Дальнейшее ведение:
– наблюдение у уролога, андролога
– контроль ОАК, ОАМ, спермограммы через 1 месяц
– ограничение физической нагрузки в течении 2-х месяцев
Индикаторы эффективности лечения и безопасности методов диагностики и лечения:
– отсутствие болевого синдрома,
– отрицательная проба Вальсальвы,
– отсутствие расширения вен гроздьевидного сплетения по УЗИ,
– устранение обратного тока крови из почечной вены в гроздьевидное сплетение.
Проба Вальсальвы при варикоцеле
 Медицина совершила значительный рывок в развитии за последние годы, что связано в том числе и с внедрением высокотехнологичных методов диагностики и хирургического устранения заболеваний.
Медицина совершила значительный рывок в развитии за последние годы, что связано в том числе и с внедрением высокотехнологичных методов диагностики и хирургического устранения заболеваний.
Данный прогресс не обошел стороной и обнаружение и лечение варикоцеле — варикозного расширения внутренней семенной вены,- которое является актуальной и серьезной проблемой для мужского здоровья.
Это заболевание обнаруживается у 2,3 — 20% пациентов фертильного возраста и с частотой 12% встречается у подростков в возрасте 10-15 лет. Опасность варикоцеле состоит в том, что болезнь негативно влияет на репродуктивную функцию мужчины, а в случае игнорирования лечения наступает бесплодие. По статистике, до 30% бездетных пар не имеют ребенка из-за этого заболевания у партнера.
Мультифакторный генезис варикоцеле обусловил необходимость проведения комплексной дооперационной диагностики для выработки адекватной хирургической методики лечения. Несмотря на популяризацию ультразвуковых технологий сканирования тестикулярного варикоза и патологий в бассейне левой почечной вены, активно применяются и приемы физикальной диагностики.
Физикальная диагностики варикоцеле
Эти приемы базируются на физиологической способности сосудов гроздевидного сплетения уменьшаться и увеличиваться в диаметре в зависимости от условий — если мужчина находится в стоячем положении, то сосуды набухают, если лежит — спадают. Путем поглаживания вены по направлению снизу-вверх уролог опорожняет артерию или наполняет ее, проводя обратные манипуляции. Обнаружить облитерированную вену в мошонке не составляет для медика труда, если болезнь прогрессирует в течение нескольких лет.

Одним из наиболее распространенных способов физикального обнаружения варикоцеле является проведение пробы Вальсальвы. При натуживании и задержке дыхания вены семенного канатика увеличиваются в объеме, что указывает на присутствие варикозного расширения. Процедура проводится в течение 10 минут. Проба Вальсальвы и другие способы проведения диагностики предполагают проведение обследования в теплом кабинете, поскольку прохладный воздух, равно как и холодные руки врача или зонд прибора, вызывают сокращение кремастера и кожного покрова мошонки, что препятствует качественному осмотру мужчины. Вне зависимости от результатов физикального осмотра пациенту назначают проведение более информативной и совершенной ультразвуковой диагностики.
Алгоритм и необходимость ультразвукового сканирования
Тогда как физикальные способы позволяют только выявить наличие варикоцеле в семенном канатике, ультразвуковое сканирование информирует о типе болезни и нарушениях в сперматогенезе, которые успел нанести недуг, дает информационную базу для назначения адекватной тактики лечения. В качестве подтверждения эффективности ультразвукового сканирования целесообразно ознакомиться с результатами одного из исследований. Работа проводилась в период 1998-2006 гг в отделении хирургии сосудов ГУ СККБ. Были обследованы и прооперированы мужчины с варикоцеле (101 пациент) в возрасте 6 — 35 лет.

Для оценки морфологического состояния ренокавальной зоны и сосудов гроздевидного сплетения применялась комплексная флебография, эхография и флеботензиометрия. Диагностика позволила выявить 3 вида гемодинамически значимого рефлюкса в вены гроздьевидного сплетения по Coolsaet, причем у 89 пациентов обнаружен первый реносперматический тип без рефлюкса, у 7 мужчин диагностирован второй илеосперматический тип и третий смешанный тип наблюдался у 5 больных.
В ходе ультразвукового исследования ренокавальной зоны пристальное внимание было уделено признакам аорто-мезентериальной компрессии левой почечной вены. На основании обследования удалось сформулировать показания к проведению реконструктивного вмешательства на левой яичковой вене.
Наряду с пробой Вальсальвы и способами ультразвуковой диагностики одной из обязательных процедур, которые проходит пациент на этапе диагностики, является анализ спермограммы. Такое исследование направлено на определение объема эякулята, процента малоподвижных, неподвижных и мертвых сперматозоидов, скорости их движения и прочих параметров, влияющих на репродуктивную функцию.
Варикоцеле у мужчин.
Варикоцеле встречается у 11 % мужского населения. Изменения в спермограмме с проблемой варикозного расширения вен семенного канатика имеются у 25 % мужчин. Болевой синдром встречается у 10 мужчин из 100 с диагнозом варикоцеле.
Варикоцеле нарушает работу клеток Лейдига, приводит к снижению объёма яичка и изменениям в спермограмме.
Анатомические предпосылки варикоцеле.
Нормальная анатомия и физиология семенного канатика и структур яичка.
Яички парный орган. Находятся в кожно — мышечном мешке — мошонке. Яички вынесены за пределы брюшной полости в связи с разными рабочими температурными режимами организма и мошонки. Ядро организма функционирует при температуре 36 — 37 °С Температурный режим мошонки отличается на 1 — 2 градус ниже температуры ядра.
Яичко находится в мобильном состоянии за счёт структур семенного канатика. Это предотвращает яичко от травматизации и способствует кровообращению в яичках. Основные составляющие семенного канатика: мышца, поднимающая яичко, семявыносящий проток, вена и артерия семявыносящего протока, вена и артерия мышцы, поднимающей яичко, собственная артерия яичка и яичковые вены в виде лозовидного сплетения (названо в связи со схожестью с виноградной), а также фасции покрывающие мышцы и лимфатические протоки. Существуют особенности яичковых вен. Левая яичковая вена проходя через паховый канал впадает в почечную вену под прямым углом, что является предрасполагающим фактором, в отличии от правой яичковой вены, которая впадает напрямую в нижнюю полую вену.
Причины варикоцеле.
Разделяют врождённые и приобретённые причины, способствующие варикоцеле.
К врождённым относятся: удвоение яичковой вены, кольцевидное строение левой почечной вены, врожденные патологии клапанного аппарата яичковой вены, врождённый стеноз почечной вены, высокий рост.
Приобретённые: повышение внутрибрюшного давления (занятия бегом, тяжёлой атлетикой хронические запоры), сдавление яичковой вены крупными сосудами. Эти состояния приводят к повышению давления в почечной вене и второстепенно в яичковой вене, так как венозное давление — это гидростатическое давление, то есть давление столба жидкости.
Диагностика варикоцеле.
В настоящее время существуют лучевые и не лучевые методы обследования.
К не лучевым методам относят: осмотр, пальпацию, термографию.
К лучевым методам относится флебография и УЗИ органов мошонки с использованием дополнительных методик.
УЗИ при варикоцеле.
В практике врача уролога — андролога УЗИ занимает первое место в диагностике варикоцеле и стало «золотым стандартом».
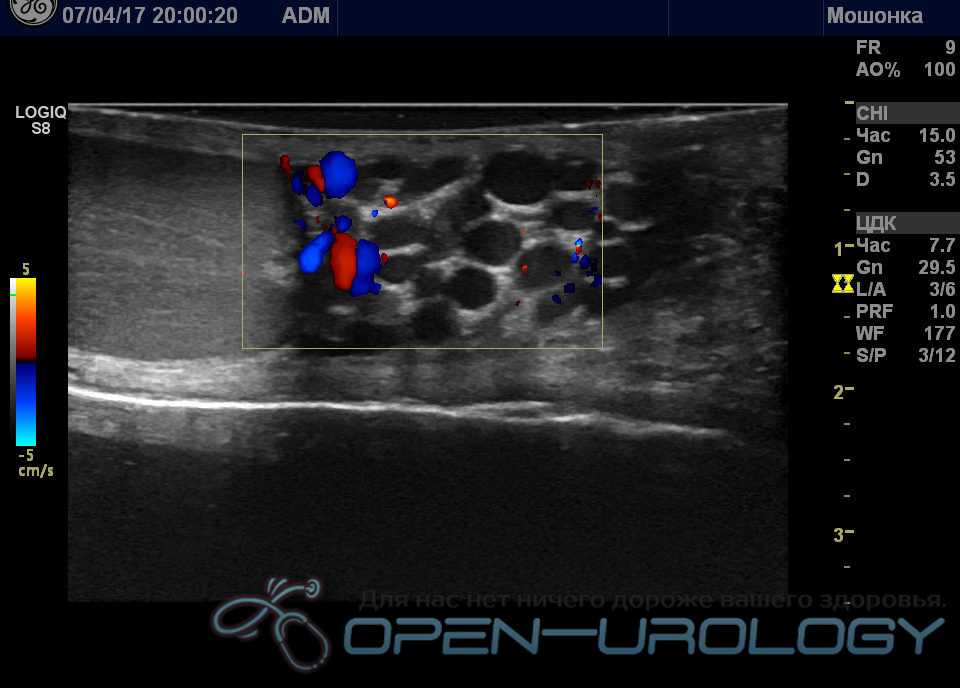 Используются современные линейные высокочастотные датчики. Для оценки анатомии используют «серую шкалу» (врач на экране видит все структуры в черно — серо — белом цвете). При данной методике выявляются трубчатые структуры в проекции пахового канала и мошонки. Это и есть вены. Измеряется диаметр вен. В норме диаметр вены не должен превышать 2 миллиметра и ход вен должен быть прямолинейным. При варикоцеле в проекции пахового канала и мошонки обнаруживается конгломерат переплетённых извитых трубчатых структур, которые как бы нависают на других элементах семенного канатика.
Используются современные линейные высокочастотные датчики. Для оценки анатомии используют «серую шкалу» (врач на экране видит все структуры в черно — серо — белом цвете). При данной методике выявляются трубчатые структуры в проекции пахового канала и мошонки. Это и есть вены. Измеряется диаметр вен. В норме диаметр вены не должен превышать 2 миллиметра и ход вен должен быть прямолинейным. При варикоцеле в проекции пахового канала и мошонки обнаруживается конгломерат переплетённых извитых трубчатых структур, которые как бы нависают на других элементах семенного канатика.
При исследовании функции вен используют дополнительные методики.
Метод цветового Доплеровского картирования (ЦДК) помогает оценить работу клапанного аппарата вен и скоростные показатели, а также время движения крови в сосуде. В норме венозный отток, то есть работа вен синхронизирована с актом дыхания и движениями диафрагмы. После вдоха на первой секунде происходит замыкание венозных клапанов и движение крови венах замедляется и скорость венозного кровотока равна нулю. На выдохе мышцы диафрагмы сокращаются и увеличивается внутригрудное давление. За счёт этих механизмов осуществляется притяжение крови к сердцу. Методика ЦДК наглядно иллюстрирует на экране фазу рефлюкса благодаря чему можно диагностировать варикоцеле.
Проба Вальсальвы
Иногда в покое рефлюкс при варикоцеле совершенно не выражен, в таких случаях требуется проведение дополнительных проб, таких как проба с натуживанием и задержкой дыхания или проба Вальсальвы.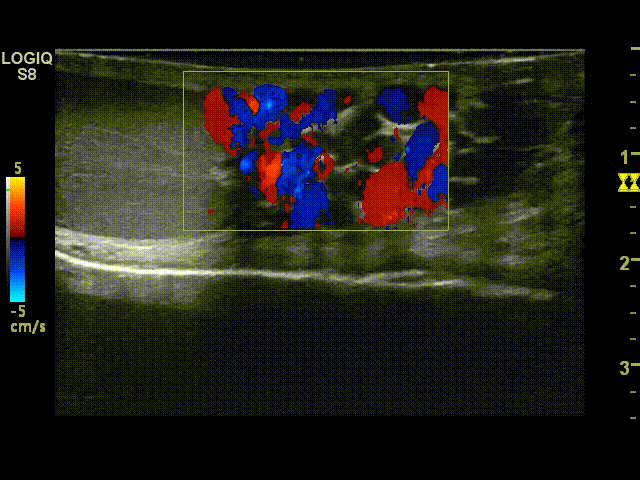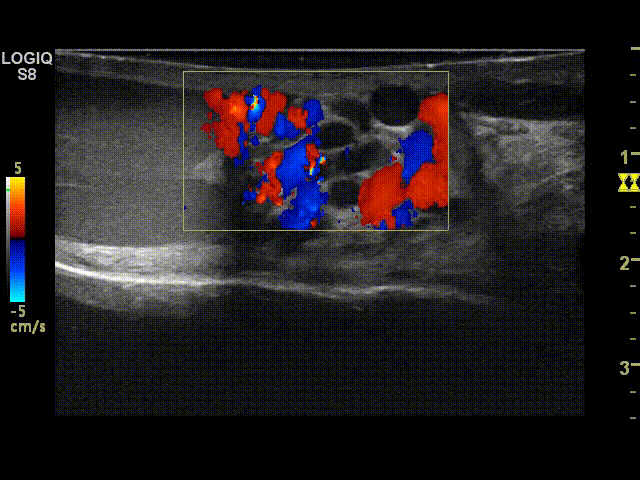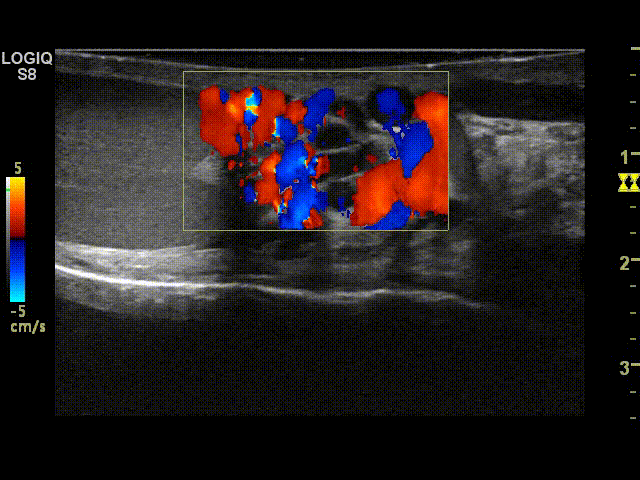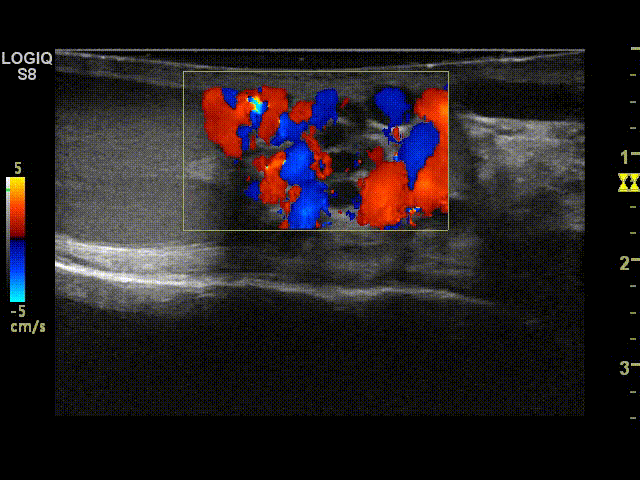
Проба Вальсальвы при варикоцеле проводится следующим образом: пациент делает глубокий вдох и начинает натуживать живот. В этот момент в режиме ЦДК врач в норме видит только пульсацию яичковой артерии и артерии семявыбрасывающего протока. При варикоцеле в режиме ЦДК визуализируются сеть изгибающихся трубчатых структур в синем и красном цвете — это и есть варикозно расширенные вены или варикоцеле. Окрашивание вен более 1 секунды говорит о неправильной работе или так называемом рефлюксе. Данное состояние выражается в проникновении крови через несостоятельные клапаны и расширенные варикозные узлы в яичко и способствует нарушению питания яичка.
После операции варикоцеле.
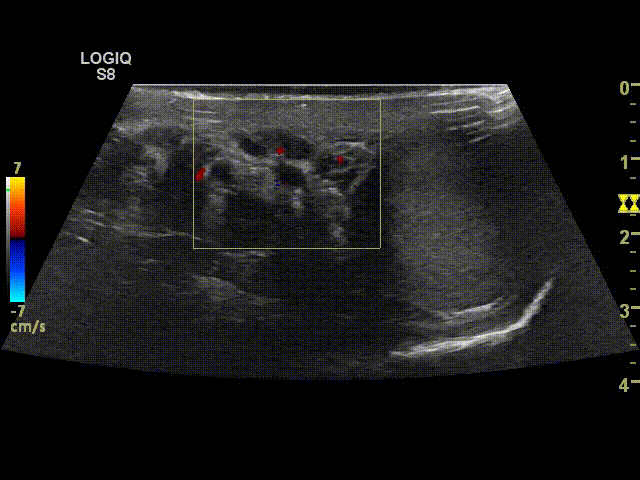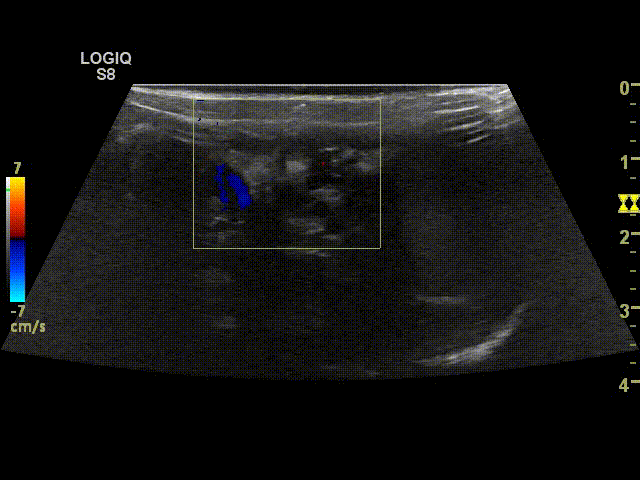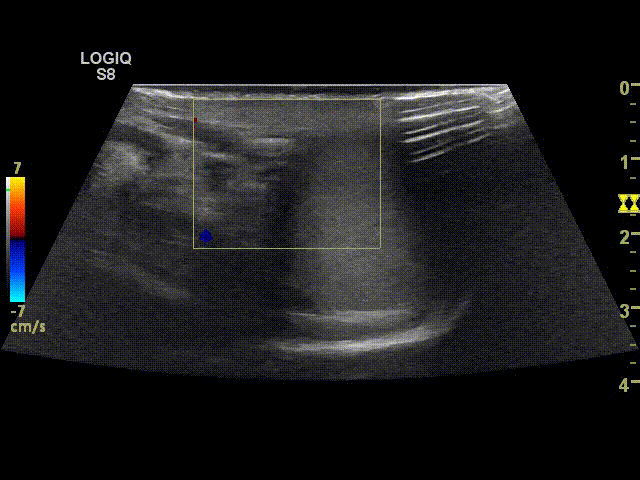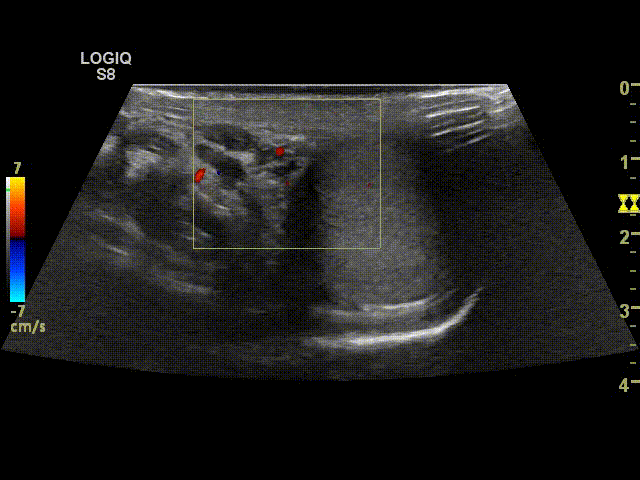
При выполнении УЗИ после проведенной операции у пациента определяются вены с гипоэхогенным содержимым. При проведении пробы Вальсальвы ретроградного кровотока быть не должно. Должна визуализироваться яичковая артерия, а также могут определяться собственные вены семявыносящего протока.
Диагностика рака простаты
 Рак предстательной железы занимает второе место по причинам смертности представителей мужского пола. Злокачественная опухоль поражает орган у каждого седьмого мужчины возрастом старше пятидесяти лет. Патологический процесс не только локализуется в простате, но и склонен к метастазированию. Современные методы диагностики позволяют выявить онкологическое заболевание на ранних стадиях даже при отсутствии характерных симптомов.
Рак предстательной железы занимает второе место по причинам смертности представителей мужского пола. Злокачественная опухоль поражает орган у каждого седьмого мужчины возрастом старше пятидесяти лет. Патологический процесс не только локализуется в простате, но и склонен к метастазированию. Современные методы диагностики позволяют выявить онкологическое заболевание на ранних стадиях даже при отсутствии характерных симптомов.
Пальпация предстательной железы через прямую кишку при раке простаты
 Благодаря близкому расположению простаты к прямой кишке уролог может провести пальцевое ректальное исследование. Простой метод позволяет выявить наличие опухоли, поскольку она отличается от других тканей неподвижностью, увеличенной плотностью. В большинстве случаев новообразования располагаются в периферической зоне, поэтому врач может нащупать их через прямую кишку.
Благодаря близкому расположению простаты к прямой кишке уролог может провести пальцевое ректальное исследование. Простой метод позволяет выявить наличие опухоли, поскольку она отличается от других тканей неподвижностью, увеличенной плотностью. В большинстве случаев новообразования располагаются в периферической зоне, поэтому врач может нащупать их через прямую кишку.
Здоровая железа имеет эластичную консистенцию, симметричные контуры и реагирует при надавливании. При пальпации врач обращает внимание на:
- асимметрию и нечеткость контуров;
- бугристость поверхности;
- неподвижность при надавливании;
- наличие плотной опухоли, выступающей в просвет кишки.
Пальцевое исследование – первичный метод диагностики, который обязательно проводится при осмотре мужчины. Результат подкрепляется лабораторными и инструментальными исследованиями.
Анализ крови на ПСА
Простатспецифический антиген – вещество, которое находится в сыворотке и предстательной железе мужчины. При аномальном увеличении объема органа уровень ПСА вырастает, поскольку происходит нарушение целостности структуры клеток. При нормальном состоянии простата защищена клеточным барьером.
ПСА увеличивается и при других заболеваниях, не связанных с раком. О раковом процессе сообщает уровень ПСА выше нормы – от 4 нг/мл и более. Также при исследовании антигена учитывают соотношение общего ПСА к свободному. Если оно составляет меньше 15%, значит, вероятность наличия рака высокая.
Пальцевое ректальное исследование, катетеризация мочевого пузыря, биопсия и массаж предстательной железы увеличивает концентрацию антигена на 3 недели. Поэтому анализ сдают через время после описанных исследований, чтобы получить достоверные результаты.

Трансректальное ультразвуковое исследование
Для диагностики рака простаты используют трансректальное УЗИ, которое проводится через прямую кишку. Исследование позволяет более точно определить наличие опухоли в отличие от абдоминального, поскольку между прямой кишкой и простатой очень тонкая стенка.
Типичное состояние при раке предстательной железы – наличие узлов гипоэхогенной структуры, преимущественно в периферической зоне простаты. При ТРУЗИ невозможно определить характер опухоли, поэтому исследование всегда дополняется пальпацией, анализом ПСА и другими диагностическими методами.

МРТ малого таза с контрастированием
Магнитно-резонансная томография – точный метод диагностики, который используется для уточнения результатов ультразвукового исследования. Для определения характера опухоли проводят МРТ с констатированием – в вену вводят препарат с парамагнетическими веществами, которые делают изображения тканей и сосудов более четкими. Злокачественная опухоль быстро накапливает контраст, после чего ее легко распознать на снимке. Мультипараметрическая МРТ безопасна для организма, введенные вещества не вызывают аллергических реакций. Томография позволяет определить расположение опухолей, степень поражения окружающих тканей. МРТ назначают при подготовке к фьюжн биопсии .
Подозрительные очаги классифицируют по шкале P irads:
- 1-2 балла – рак отсутствует.
- 3-4 бала – возможная онкология.
- 5 баллов – высокий риск рака.
Дополнительные методы исследования
Для диагностики рака простаты при определенных показаниях дополнительно назначают компьютерную томографию, ПЭТ-КТ, радиоизотопное сканирование
- ПЭТ-КТ проводится с помощью введения в вену радиофармпрепарата для выявления опухоли и метастазов. На ранних стадиях метод неинформативен. Исследование делают при умеренном и высоком онкологическом риске, так же, в дополнении к остеосцинтиграфии или с целью исключения рецидива после простатэктомии.
- КТ позволяет исключить наличие метастазов в кости, брюшной полости, легких и других органах. Зачастую, при наличии противопоказаний к МРТ, пациентам выполняют КТ органов малого таза с контрастированием для оценки распространенности процесса.
- Радиоизотопное сканирование (сцинтиграфия) – метод диагностики, который назначают при умеренном и высоком онкологическом риске с целью исключить наличие метастазов. Для процедуры пациенту вводят в вену радиоактивный препарат. Через три часа тело сканируют с помощью гамма-камеры, которая передает информацию на компьютер.
Биопсия простаты
 Любое подозрение на онкологию: отклонение ПСА от нормы, прощупывание узлов при пальцевом обследовании, даже при нормальном уровне антигена, обнаружение гипоэхогенных участков при УЗИ, должно быть верифицировано с помощью биопсии. Это информативный метод диагностики, который подразумевает получение образцов тканей из железы для дальнейшего исследования.
Любое подозрение на онкологию: отклонение ПСА от нормы, прощупывание узлов при пальцевом обследовании, даже при нормальном уровне антигена, обнаружение гипоэхогенных участков при УЗИ, должно быть верифицировано с помощью биопсии. Это информативный метод диагностики, который подразумевает получение образцов тканей из железы для дальнейшего исследования.
Существует несколько видов биопсии: трансректальная, сатурационная, фьюжн.
Золотой стандарт – трансректальная биопсия
Распространенный метод забора биоптатов из предстательной железы мужчины. Особенности трансректальной биопсии:
- Проводится под контролем УЗИ через прямую кишку.
- Врач делает 12 проколов иглой с режущими концами, на которых остаются частички тканей. Их консервируют и отправляют на экспертизу.
- Трансректальное вмешательство минимально травмирует ткани.
Недостатком считается то, что есть вероятность получения недостаточного количества биоптатов, что приводит к необходимости проведения повторной биопсии.
Расширенная сатурационная биопсия простаты
П олучение образцов тканей из предстательной железы также проводится под контролем УЗИ.
- При сатурационной биопсии ультразвуковой датчик вводится в прямую кишку.
- Проколы делают через промежность – это увеличивает шансы на получение более информативных биоптатов.
- При сатурационной биопсии врач делает забор образцов из 24 и более разных точек.
- Процедура выполняется под спинномозговой анестезией.
Фьюжн биопсия – самый информативный метод диагностики рака простаты
Fusion-биопсия подразумевает выполнение прицельных проколов в 3-4 подозрительные точки. Процедура проводится под контролем УЗИ и МРТ с констатированием. Снимки накладывают друг на друга для получения трехмерного изображения простаты. Это позволяет точно определить локализацию участка для забора тканей. Преимущества фьюжн биопсии:
- Прицельные проколы в подозрительные точки.
- Высокая точность диагностики – 95%.
- Отсутствие боли за счет эпидуральной анестезии.
- Сохранение целостности стенок кишечника
Целевые группы риска, которые должны проходить диагностику
Обследование для определения наличия рака простаты на ранних этапах его развития необходимо проводить среди мужчин, которые относятся к целевым группам риска:
- Возрастом 45 -70 лет. В этот период происходит изменение уровня гормонов, обостряются хронические болезни, что может приводить к патологическим делениям клеток железы.
- После сорока лет, среди мужчин, у которых отец или братья имели рак простаты.
Особенности диагностики рака простаты в пожилом возрасте
Мужчинам после 70-ти лет нет необходимости проводить раннюю диагностику рака простаты. В этом возрасте чаще обнаруживается медленно прогрессирующая патология, которая не влечет серьезных последствий.
Биопсия для пациентов пожилого возраста опасна тем, что может привести к побочным эффектам в виде проблем с мочеиспусканием, инфекции, кровотечению и т.д. Урологи в таком случае ориентируются на показатели уровня ПСА и сопутствующие симптомы. При слабо выраженных признаках чаще отказываются от инвазивной диагностики и выбирают тактику наблюдения при помощи МРТ и ПСА.
Врач индивидуально определяет необходимые методы для исследования состояния предстательной железы. Мужчинам важно внимательно следить за организмом и при первых подозрениях наличия проблем с простатой обращаться к специалисту.
Ранняя диагностика и лечение рака предстательной железы

В Москве кардинально изменилась ситуация с раком предстательной железы: благодаря робот-ассистированной операции и другим видам вмешательства у пациентов появилась возможность полностью вылечить онкологическое заболевание, сохранив при этом все важные функции организма. Главное условие эффективной терапии рака предстательной железы – диагностика на ранних стадиях.
Модернизация московского здравоохранения привела к нескольким серьезным изменениям в области урологии. Первое – биопсия предстательной железы под контролем ультразвука заменила биопсию органа под контролем пальцем. Второе – все урологи, которые делают биопсию, обучены делать это на самом современном уровне. Третье – модернизация привела к тому, что существуют центры, которые смотрят биоптаты (материалы, полученные методом биопсии), используя оценку по шкале Глисона. Благодаря модернизации столичного здравоохранения во всех клиниках установлены аппараты МРТ, которые в случае необходимости позволяют смотреть простату – процедуру можно назвать дополнительной диагностикой. Наконец, модернизация привела к тому, что существуют роботическая программа, брахитерапия, а также лучевая терапия, которая воздействует непосредственно на предстательную железу, а не на соседние органы.

Рак предстательной железы – это, во-первых, самое частое онкологическое заболевание у мужчин, которое диагностируется у каждого седьмого представителя сильного пола в мире. Во-вторых, рак предстательной железы, аденома предстательной железы, хронический простатит, заболевания, передающиеся половым путем, – разные вещи. Рак предстательной железы – это редкое заболевание у мужчин до 45 лет, поэтому пациенты должены понимать, что диагностика, исследование и обследование на опухоль в подавляющем большинстве случаев начинаются в 45 лет.
К сожалению, рак предстательной железы невозможно предотвратить, причины его происхождения также неясны – заболевание принято считать болезнью цивилизации.
Сегодня ранняя диагностика рака предстательной железы (не скрининг, а ранняя диагностика) – процедура не страшная и простая. Она предполагает анализ крови на уровень простатического специфического антигена (ПСА), который ежегодно выполняется каждому мужчине с 45 лет и предусматривает забор крови из вены. За сутки до анализа мы не рекомендуем прием алкоголя, половое сношение и физическую активность, связанную с седлом – катание на велосипеде, езду на лошади. Это простые, но важные факты. После анализа крови на ПСА врач-уролог поликлиники проводит пальцевое ректальное исследование предстательной железы.
Необходимо понимать, что ректальное исследование предстательной железы выполняется после взятия ПСА, поскольку брать анализ после ректального исследования в течение какого-то времени не рекомендуется. После пальцевого ректального исследования проводится ультразвуковое обследование предстательной железы, измерение ее объема и определение состояния мочевыделительной функции – если имеются жалобы на расстройство мочеиспускания.
Следующий важный факт, о котором должен знать мужчина, состоит в том, что на ранних стадиях рак предстательной железы не вызывает никаких симптомов. Поэтому отсутствие беспокойств, жалоб, болей не имеет никакого отношения к диагнозу. Он может быть поставлен на ранней стадии Т1 или Т2, когда опухоль не вышла за пределы предстательной железы, находится внутри нее – в этом случае мы потенциально можем избавить больного от злокачественной опухоли, удалив предстательную железу. Например, у 99% больных никаких жалоб при этом нет.
В начале 80-х годов, до эры ПСА, превалировали стадии рака предстательной железы Т3 и Т4 – до них человека, как правило, ничего не беспокоило. Люди обращались лишь в тот момент, когда появлялась боль, другие симптомы – на глубоко запущенных стадиях заболевания.
Сегодня рак предстательной железы на ранних стадиях – это излечимый рак, который не приостанавливается, а полностью вылечивается. На данный момент существует не так много излечимых онкологических заболеваний.
Ранняя диагностика рака предстательной железы
Что необходимо для постановки диагноза «рак предстательной железы»? Во-первых, врач-уролог должен определить, есть ли показания к проведению биопсии. Повышенные показатели ПСА (сегодня мы говорим о том, что ПСА должен быть не больше 2,5–3 нанограммов на миллилитр), подозрения при пальцевом ректальном исследовании или проведении ультразвука – наличие одного из трех указанных условий диктуют необходимость биопсии предстательной железы.
Биопсия предстательной железы – это методика игольного забора ткани простаты из 12–16 точек, которая выполняется врачом-урологом под местной анестезией и не требует госпитализации. Все урологи Москвы в поликлиниках, стационарах кратковременного пребывания, консультативно-диагностических центрах в той или иной степени выполняют биопсию предстательной железы. Мужчина может выбрать место, где пройдет процедуру.
Биопсию делают под контролем ультразвукового исследования. В зависимости от результатов процедуры врач-уролог ставит диагноз, и больной выбирает один из предложенных вариантов лечения.
Если мы исключаем рак простаты, больному нужно наблюдаться дальше.
Если обнаружена стадия рака предстательной железы Т1 или Т2 – необходимо радикальное лечение: удаление простаты, брахитерапия – внедрение в орган радиоактивных зерен, либо дистанционная лучевая терапия. Все методы лечения рекомендованы Российским обществом урологов, Российским обществом онкоурологов, Европейской ассоциацией урологов и Международным урологическим обществом.
В случае если мы подозреваем у больного стадию Т3, вопрос нужно решать в каждом индивидуальном случае по-разному. Речь может идти о мультимодальной терапии, предусматривающей удаление простаты, лимфоузлов и дальнейшее облучение этой зоны с применением гормонотерапии. Можно сделать облучение без удаления простаты и также провести гормонотерапию. Решение о терапии принимается совместно с онкологом-радиологом.
Что же касается стадии Т4, когда есть отдаленные метастазы, – к сожалению, приходится начинать с гормонотерапии и продолжать наблюдение больного непосредственно в условиях онкологического учреждения, которое занимается гормонотерапией и дальнейшей химиотерапией данного пациента.
Что если ПСА высокий, но биопсия не выявила рак предстательной железы? Обследование продолжается с помощью магнитно-резонансной томографии (ее также делают практически всем пациентам перед операцией). МРТ в данном случае выполняется не для диагностики, а для ориентации, непосредственной оценки предстательной железы, взаимодействия простаты с остальными органами. Что касается МРТ в плане диагностики – она приходит на помощь, когда мы сомневаемся в том, делать ли биопсию, развивается ли в органе онкологический процесс, не знаем, что происходит с предстательной железой.
Наряду с МРТ и независимо от результатов биопсии мы часто назначаем антибактериальную терапию, думая, что у пациента воспалительный процесс. Если ПСА остается высоким, биопсию повторяют в расширенном формате.
Важно понимать, что МРТ никогда не заменит биопсию: по результатам томографии нельзя поставить диагноз – МРТ может только заподозрить и оценить структуру, но морфологическую структуру она оценить не может – для этого нужна биопсия предстательной железы.
Благодаря ранней диагностике повысилась выявляемость рака предстательной железы на локализованных стадиях, когда есть возможность сохранить все жизненно важные функции организма.
Радикальная простатэктомия
Операция по удалению предстательной железы вместе с окружающей клетчаткой и лимфоузлами называется радикальной простатэктомией. Она выполняется открытым, лапароскопическим или робот-ассистированным способом. Наиболее щадящий способ, сохраняющий все структуры и функции, – это робот-ассистированная операция.
Сегодня в четырех медицинских учреждениях Москвы существуют успешно работающие роботические программы. Речь идет о Московском клиническом научном центре, Городской клинической больнице № 31, Городской клинической больнице имени С.П. Боткина и Городской клинической больнице имени С.И. Спасокукоцкого. В этих клиниках работает около десяти бригад.
Робот-ассистированные операции выполняются на разных условиях, в том числе по квоте на оказание высокотехнологичной медицинской помощи.
Также в Москве достаточно активно применяется брахитерапия – метод лучевой терапии, предполагающий внедрение в орган облучающих зерен, которые лечат рак предстательной железы.
При лучевой терапии орган не удаляют, при операции же происходит обратное.
Важно сказать, что робот-ассистированная операция позволяет сохранить эректильную функцию пациента (после оперативного вмешательства она меняется), функцию удержания мочи, что также возможно и при открытой операции, но в меньшей степени. После лучевой терапии эректильная функция не сохраняется.
Робот-ассистированная операция – наиболее щадящее вмешательство, которое переносится пациентом легче, с минимальной кровопотерей. Открытые операции, к слову, проводят сегодня все реже и реже.
Когда пациент приходит в больницу, у него спрашивают: «Что вы хотите?», на что он отвечает: «Я не доктор – вы мне скажите». Но здоровье принадлежит пациенту, и только после длительных многократных бесед с больным, его родственниками мы принимаем взвешенное решение о том или ином виде терапии.
Рак простаты – это не приговор: вопрос репродуктивной функции и зачатия можно решить с помощью криоконсервации эякулята до операции либо, если это не сделано по каким-то причинам, экстракции сперматозоида из яичка или придатка – это вспомогательная методика для дальнейшего искусственного оплодотворения. Существуют урологи, которые непосредственно занимаются этим, работая в разных медицинских центрах Москвы.
Сегодня есть возможность наблюдать пациентов, которым поставлен диагноз «рак предстательной железы». Мы делаем это в исключительных случаях, потому что международные данные и данные, которые приводятся в литературе, противоречивы. Россия в целом и Москва в частности не имели многолетнего опыта скрининга рака предстательной железы, поэтому мы не знаем до конца особенностей его развития. В связи с этим мы можем применять активное наблюдение лишь в исключительных случаях, когда уверены в том, что рак у данного пациента развиваться не будет. И второй очень важный момент – пациента нужно информировать. Опыт показывает, что незначительное количество больных готово к тому, чтобы просто наблюдать за этим заболеванием, но большинство из них хочет избавиться от рака предстательной железы. И все же мы наблюдаем больных с низким риском. В первую очередь это пациенты старших возрастных групп, например, старше 75 лет, у которых незначительно повышены показатели ПСА, а при биопсии обнаружен рак.
Жизнь без предстательной железы – не то же самое, что жизнь без сердца или печени, после операции человек не становится инвалидом. Мы понимаем, что орган очень важен, но также должны учитывать, что около 15% мужского населения земного шара старше 50 лет живет без простаты и никаких неудобств по этому поводу не испытывает.





